上部消化管用スコープ編
食道病変の内視鏡診断におけるEndocytoの有用性と活用のコツ

郷田 憲一 先生
[昭和大学江東豊洲病院 消化器センター]
I. Endocytoがもたらす臨床的有用性
生体内の細胞観察によって確信度の高い内視鏡診断が可能に
従来、消化管病変の確定診断を得るには、生検により採取された検体標本の病理組織検査を顕微鏡下で行うしかありませんでした。最大倍率520倍(OEV262H使用時)を実現した超拡大内視鏡Endocytoの上部消化管用スコープは、核・細胞の2重染色後、細胞レベルでの生体内観察によって、組織学的所見を直接とらえることを可能にしました。これにより内視鏡医は、最大80~100倍程度の従来の拡大内視鏡観察よりも確信度の高い内視鏡診断が可能になると考えられます。
食道病変の診断において、Endocytoを用いた超拡大内視鏡(endocytoscopy:EC)観察が特に有用性を発揮すると期待されるのは、癌・非癌の鑑別です。例えば、近年、腫瘍径1~3mm程度の超微小癌の存在が注目されるようになっています1)。これらは極めて早期であるため、組織学的に癌であっても、拡大NBI観察でとらえられる上皮乳頭内血管ループ(intraepithelial papillary capillary loop:IPCL)の形態学的異常は軽度にとどまることがあります。また、生検を試みても病変が極小であるため、適切な組織標本の作製が困難なことがあります。しかしEC観察であれば、極小病変全体の核・細胞異型をとらえて的確に診断できる可能性があります。
EC-NBI観察による血管所見が深達度診断に役立つ可能性
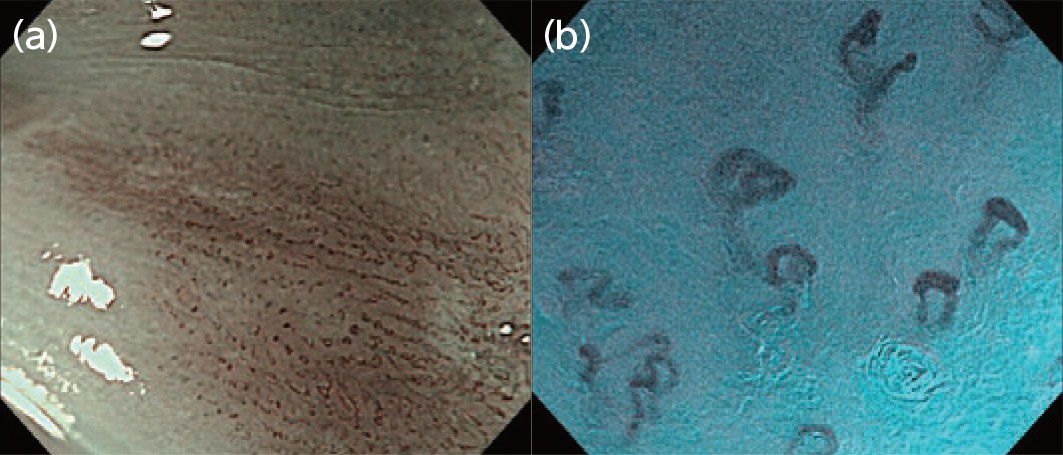
食道癌の深達度診断において、Endocytoで核・細胞を観察しても、従来の拡大NBI観察による表在血管に基づいた深達度診断の精度を向上させるメリットは期待できないと考えられています。ただしNBIとEndocytoとを併用するEC-NBI観察では、拡大NBI像の約5倍まで拡大された血管像が得られます(図3)。それにより、1本1本の血管が明瞭に視認可能となります。表在癌部の血管径はその深達度と相関することが報告されており2)、日本食道学会分類では、SM2以深を示唆する所見とされるB3血管が血管径60μm以上と定義されています3)。しかし、それらの血管径は病理組織標本上で測定されており、生体内で測定されたものではありません。したがってEC-NBI観察によって正確に血管径を測定できれば、術前の生体内における深達度と血管径との関連性を追究できる可能性が考えられます。
II. Endocytoによる観察の手順とコツ
良好な核・細胞染色像を得るには
食道でのEC観察により有用な診断情報を取得するには、目的部位の良好な核・細胞染色像を得ることが重要です。
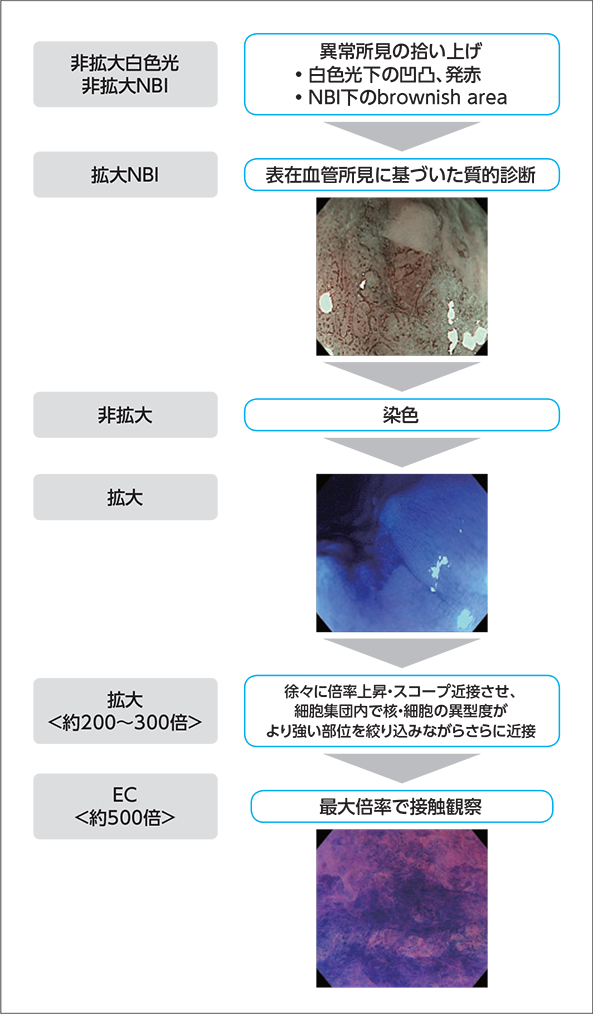
染色の手順(表)としては、まず非拡大の白色光下で凹凸や発赤、あるいはNBI下で茶褐色調領域(brownish area)といった異常所見を拾い上げ、拡大NBI観察で表在血管所見に基づいた質的診断を行います。その後、診断の確信度をより上げるため、非拡大まで倍率を戻し、病変部とその周囲を含めて染色液を撒布します。
|
① 拡大NBI観察による質的診断後、非拡大白色光観察に戻す。 |
表 食道のEC観察における核・細胞染色の手順
私どもは染色液として0.05%クリスタルバイオレット10ccと1%メチレンブルー1ccの混合液11ccを作製し使用しています4)。過去の報告で1%メチレンブルーによる生体内染色で遺伝子異常が惹起されるリスクが示された5)ことから、安全性を確保するために極めて低濃度(0.1%以下)のメチレンブルーを用いています。染色液撒布前には、50~60ccの送水で粘膜表面に付着する粘液を洗浄します。染色液が希釈されて染色不十分になるのを防止するため、洗浄後に残存した水は必ず吸引して完全除去します。作製した染色液を1回量1~2cc撒布した後、徐々に倍率を上げて目的部位を絞り込み、EC観察を開始しますが、撒布から1~2分程度経過しても染色が不十分であれば染色液を追加撒布します(図4)。食道では多くの場合、1回の撒布で十分良好な染色が得られますが、胃・十二指腸の病変はやや染色されにくい傾向があります。食道内に貯留した染色液の吸引除去は原則として行いません。その理由として、残存染色液により細胞の染色性が進むメリットが期待できるうえ、吸引により粘膜表層の細胞が剝離してレンズに付着した場合、画質の劣化につながる懸念があるためです。最も観察に適した染色像が得られるのはEC観察開始2〜3分後とされ、それ以降は時間経過とともに粘膜表層からの細胞剝離が進んでしまうため、約5分間で集中して良質のEC観察画像を取得するよう心掛けます。
なお、EndocytoでのEC観察時には、内視鏡システムのビデオプロセッサーで色調調整の設定を赤-8、青+8としています。これにより核・細胞染色像が強調され、メチレンブルーを低濃度とした染色液を使用しても、診断に適したEndocyto像を得ることが可能となります。
Endocytoのスコープ操作法(アプローチと倍率調節)
Endocytoでは、非拡大から最大倍率520倍まで、一連の倍率調節をズームレバー操作で行います。従来の拡大内視鏡(最大倍率約100倍)よりも繊細なレバー操作が求められますが、ズーム式を採用したことにより、通常観察、そして従来の拡大NBI観察と徐々に倍率を上げながら、ターゲット(Endocytoで観察したい部位)を絞り込んでいくことが可能です。
具体的な手順(図5)として、染色前の拡大NBI観察で異常血管を認めた部位に対し、細胞の視認はできない倍率約100倍から、数百個程度の細胞集団が視認できる200~300倍まで、スコープを徐々に近接させながら倍率を上げていきます。その細胞集団内で、構造・細胞の異型度がより強い部位を絞り込みながらさらに近接し、最終的には接触観察し、最大倍率まで上げたところでEC画像を取得します。
このように最大倍率での接触観察まで、スコープのアプローチと倍率調節を同時かつ緩徐に行うことで、ターゲットを見失いにくいだけでなく、粘膜からの出血も起こしにくいメリットがあると考えられます。EC観察下で出血を来した場合、赤血球が1個単位で視認され、観察視野が著しく妨げられてしまいます。もし倍率を上げている途中でターゲットを見失った場合には、いったん倍率を下げて遠景から再度アプローチし直す必要があります。その際も急激な倍率調節は避け、徐々にスコープを粘膜面から離しつつ倍率を下げ、ターゲットを視野内にとらえ直したところで、再び倍率を上げながら近接から接触し、観察部位の絞り込みを行うようにします。
ただ狭小かつ直線的な管腔臓器である食道では、病変に対し接線方向からのアプローチにならざるを得ません。そこで近接・接触の際は吸気し、食道壁の伸展性を下げることによって粘膜面の柔軟性を高めます。すると粘膜面がスコープ先端を軽く押し当てるだけで変形するため、接触観察が可能となります。しかし200~300倍の観察で、粘膜に接触しないスコープ位置で焦点距離を安定させて良好な静止画像を取得するのは通常、困難です。この倍率では、観察しながら絞り込むべき構造異型の高い部位に見当を付けることが重要と考えます。
正常粘膜との比較により病変部の特徴をとらえる
EC診断のプロセスは、通常内視鏡診断と同様、比較診断学に基づいています。
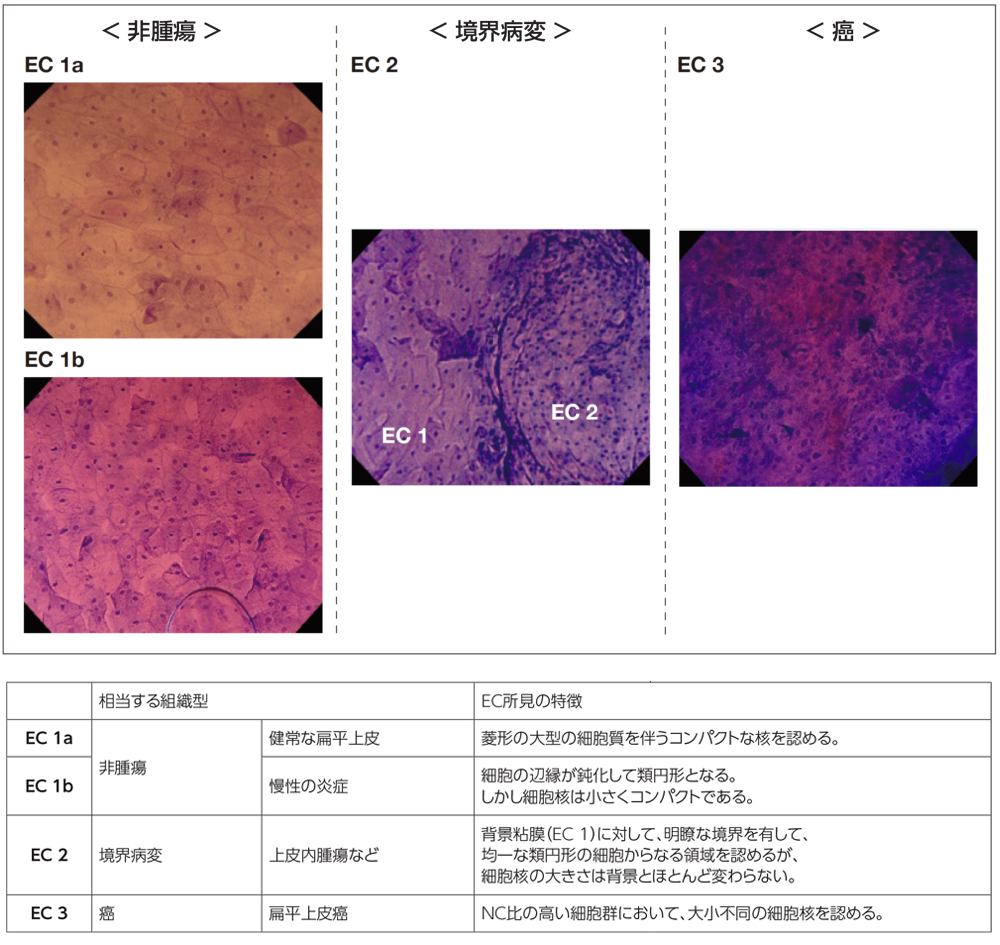
食道病変の内視鏡診断をEC像に基づいて行うには、EC分類(p.2:図2)が有用です。食道には腺構造がないため、核の密度、大きさ、形状を順次評価することで診断を進められるシンプルな診断体系をなしており、習得しやすいと考えます。
ただそれには、従来の拡大内視鏡よりはるかに高い倍率でのEC観察画像に慣れることが重要です。そのコツとして、病変部を周囲の正常粘膜も含めて十分に染色させた後、病変との境界部において、まず正常粘膜の核の密度、大きさ、形状をよく観察し、それらのイメージをインプットします。その後、徐々に病変の内側に入りながら、正常粘膜のEC像と比較することにより、明瞭な境界の有無と、病変内のEC像(特に細胞の形状と核の大きさ・大小不同)についての特徴をとらえていけば、比較的容易にEC分類に基づく評価・診断が行えると思います。
なお、接触観察となる最大倍率時のEC観察では、拡大レンズと粘膜面との間に照明光が入り込むスペースがないため、光量不足により画像が暗くなりやすい印象があります。そこで、シリコーンゴム製の先端アタッチメントを内視鏡先端部に対して傾斜を付けて装着し(ビニールテープでしっかりと固定)、照明レンズ側に間隙を設けることで、接触観察時にレンズ面に入る照明光が確保されるよう工夫しています。
III. Endocytoのさらなる有用性への期待
NBI陰性早期癌発見や非びらん性胃食道逆流症診断への応用
今後の検討次第では、上部消化管の内視鏡診断に対するEC観察のさらなる有用性が示される可能性もあると思います。例えば、食道癌の内視鏡治療後のフォローアップに関しては、私どもの行った研究の結果、ヨード染色で多発ヨード不染を呈する食道(いわゆる「まだら食道」)では、ヨード染色に比べて拡大NBI観察のほうで、前・早期癌病変の見落としリスクが上がる可能性が示唆されています6)。拡大NBI観察による血管診断のみでは検出できない前・早期癌病変も、EC観察を加えれば何らかの細胞異型が認められ、最適な検査間隔への変更、それらの見落としリスクの軽減に結び付けられるかもしれません。また、胃食道逆流症では従来の内視鏡検査所見では異常がみられないものの、胸焼けや呑酸の症状が現れることがあります。こうした症例にEC観察を行い、扁平上皮層内への炎症細胞浸潤など組織学的レベルの異常を検出し、内視鏡的に診断できるようになるかもしれません。
他方、胃のEC観察に関しては、食道と同様にクリスタルバイオレット・メチレンブルー混合液を用いた2重染色法が試みられているものの、十分な染色が得られにくい点が課題です。しかし将来的には、大腸において開発中の自動診断システム7)が、胃に応用・実用化されれば、胃においても、Endocytoの内視鏡診断によって生検診断と同等に癌・非癌鑑別の確定診断が行えるようになると期待しています。
[ 文 献 ]
1) Goda K, Dobashi A, Yoshimura N, et al. Clinicopathological features of narrow-band imaging endoscopy and immunohistochemistry in ultraminute esophageal squamous neoplasms. Dis Esophagus 2014; 27: 267-275.
2) Santi EG, Inoue H, Ikeda H, et al. Microvascular caliber changes in intramucosal and submucosally invasive esophageal cancer. Endoscopy 2013; 45: 585-588.
3) Oyama T, Inoue H, Arima M, et al. Prediction of the invasion depth of superficial squamous cell carcinoma based on microvesselmorphology: magnifying endoscopic classification of the Japan Esophageal Society. Esophagus 2017; 14: 105-112.
4) 井上晴洋, 横山顕礼, 工藤進英. 超・拡大内視鏡―エンドサイトにおける’CM2重染色’の開発と安全性について. 日本臨床 2010; 68: 1247-1252.
5) Olliver JR, Wild CP, Sahay P, et al. Chromoendoscopy with methylene blue and associated DNA damage in Barrett’s oesophagus. Lancet 2003; 362: 373-374.
6) Goda K, Dobashi A, Yoshimura N, et al. Narrow-band imaging magnifying endoscopy versus lugol chromoendoscopy with pink-color sign assessment in the diagnosis of superficial esophageal squamous neoplasms: a randomised noninferiority trial. Gastroenterol Res Pract 2015; 2015:639462.
7) Misawa M, Kudo SE, Mori Y, et al. Characterization of colorectal lesions using a computer-aided diagnostic system for narrow-band imaging endocytoscopy. Gastroenterology 2016; 150: 1531-1532.